新傾向問題は「誘導にのれるか」が勝負の鍵です。 2008-10-27
新傾向問題は「誘導にのれるか」が勝負の鍵です。

すべての物質は、原子と呼ばれる非常に小さな粒でできています。私たちの身のまわりにある空気の中にも様々な気体が存在していますが、それらの気体もすべて、原子がもととなってできているのです。そして、原子どうしが互いに結びつくことで分子と呼ばれるかたまりを作っています。
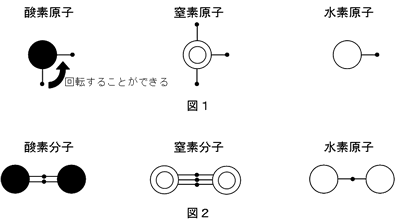
ここで、すべての原子からはそれぞれ決まった数の棒が出ており、この棒どうしが結びつくことで分子ができているものと考えてみます。つまり、人が手を伸ばして握手するのと同じように、原子どうしが結びついてるのです。このことから、原子から出ている棒を「結合の手」と呼ぶことにします。
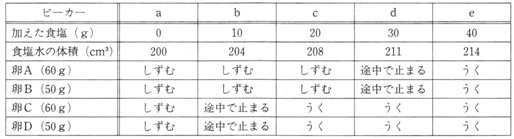
例えば、水素、酸素、窒素などの気体は、それぞれ図1のような水素原子、酸素原子、窒素原子が2つずつ結びついてできており、それらの結びつき方を表したのが図2です。ただし窒素分子はここでは表わされていません。また、以下の問いでは考えやすくするために、下記のような決まりを作ります。
<決まり>
・すべての原子の結合の手は、2本以上が同じところから出ることはない。
・それぞれの結合の手が結びつくときは、必ずまっすぐに結びつく。
・それぞれの結合の手は、まっすぐに結びつくために90°だけ回転することができる。
・原子が分子をつくるとき、すべての結合の手が結びつき、結合の手があまることはない。
また、異なった原子が結びついて、別の物質を作ることもあります。
例えば、水は水素原子2つと酸素原子1つが図3のように結びついてできています。また、図4は炭素原子をあらわしていますが、結合の手は表されていません。

問1 アンモニアは、窒素原子1つと水素原子3つが結びついてできています。このとき、アンモニア分子はどのように表されますか。
問2 メタンは、炭素原子1つと水素原子4つが結びついてできています。このことから、炭素原子には結合の手が何本あると考えられますか。
問3 二酸化炭素が水にとけると、炭酸水という水溶液になります。つまり、二酸化炭素分子と水分子が結びつくことで炭酸水となるのです。そして、炭酸水分子は図5のように原子が配置されていることがわかっています。このとき、結合の手はどのようになっていますか。
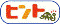
ただ「決まり」に従うだけです。

問1
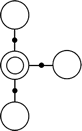
問2 4本
問3

問1 水素原子は、結合の手が1本しかないため、2つ以上の原子と結びつくことができません。つまり、水素原子どうしが結びつくことは考えられない(それで水素分子になってしまう)ので、水素原子はすべて窒素原子と結びつかなければなりません。
問2 問1と同様に、水素原子はすべて炭素原子と結びつくと考えられます。水素原子が4つ結びつくためには、炭素原子には4本の結合の手が必要です。
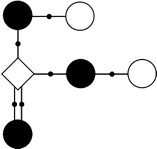
問3 まず、下の図のようにそれぞれの原子にA~Fの記号をつけて説明することにします。
1)Fの水素原子は、結合の手が1本であるためにEと結合しなければなりません。よって、ここでEの結合の手が1本使われます。
【Fの結合終了】
2)Eの残ったもう1本の結合の手は、BかDと結合することになりますが、仮にDと結合した場合、D、E、Fの結合の手がすべて使われてしまい、A~Cの原子と結びつくことができなくなってまいます。よって、Eの残りの結合の手は、Bと結びつくしかありません。
【Eの結合終了】
3)Dの水素原子は、Eと結合できないので、Aと結合するしかありません。
【Dの結合終了】
4)Aの残ったもう1本の結合の手は、Bと結合するしかありません。
【Aの結合終了】
5)残ったBとCは、それぞれ2本ずつ結合の手があまっているので、ここで2本ずつ結びつくことがわかります。
【すべての結合終了】
-------------------------------------------------------------------------------------------------------
~2箇所でブログランキングに参加しています~
1.
2.![]()
-------------------------------------------------------------------------------------------------------
ところで、こんなのはじめました。
参考書選びの参考にご利用ください。
ロジム2階参考書コーナー